SOFC(固体酸化物型燃料電池)の基礎知識
※2005年春現在の知識を基に作成されました。 ※本ページは個人の学習用として制作されたものであって、内容の信憑性は保証しません。 1.燃料電池とは 水素などの燃料から電気を作る装置のこと。水を電気分解すると、水素と酸素に分かれるが、燃料電池はその逆の発想。つまり、水素などの燃料と酸素の反応を利用して、電気を作る(結果として水が生成する)装置。 2.燃料電池の種類と特徴 燃料電池は電解質の種類によって、以下の4つに分類される。運転温度(=セル温度)、燃料は代表的なもの。 ・PEFC (Polymer Electrolyte Fuel Cell / 固体高分子型燃料電池) ※ 電解質:樹脂などの高分子膜 運転温度:20 - 100℃前後 燃料:水素、メタノール 導電イオン:H+ ※DMFC (Direct Methanol Fuel Cell) もPEFCの一種。 ※PEFCはPEM (Polymer Electrolyte Membrane)とも言われる。 ・PAFC (Phosphoric Acid Fuel Cell / リン酸型燃料電池) 電解質:リン酸水溶液 運転温度:150 - 200℃ 燃料:水素 導電イオン:H+ 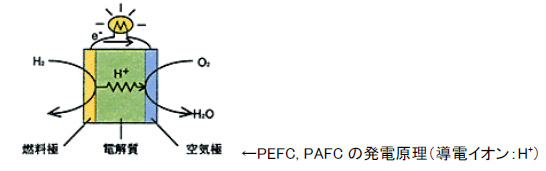 ・MCFC (Molten Carbonate Fuel Cell / 溶融炭酸塩型燃料電池) 電解質:炭素塩(炭酸リチウム、炭酸カリウム) 運転温度:650-700℃ 燃料:水素、天然ガスなど 導電イオン:CO32- ・SOFC (Solid Oxide Fuel Cell/ 固体酸化物型燃料電池) 電解質:固体酸化物 運転温度:650 -1000℃ 燃料:水素、天然ガスなど 導電イオン:O2- 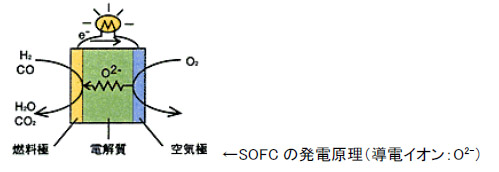 現在、開発・商品化が一番進んでいるのはMCFCであるが、低温で扱いやすいPEFC (一部商品化) と、高効率のSOFCの開発が注目を浴びている。 ■ PEFCの長所と短所 ・低温作動。 ・起動時間が比較的短い。 ・高分子材料のため、部品成型が容易でコストがかからない。 ・SOFCに比べて低効率。(水素燃料で45~55%) ・オーバーヒートに注意が必要。 ・水素燃料を使うため、インフラが問題。(都市ガスからの水素生成には別途改質機が必要。また、燃料電池車向けには、水素ステーションが必要) ・白金触媒が高価。 ■ SOFCの長所と短所 ・PEFCに比べて高効率。(天然ガス+ハイブリッド発電で55~65%) ・廃棄熱を利用してタービン発電(ハイブリッド発電)や給湯も可能。 ・都市ガスも利用可能(セルの排熱を利用した改質)で、現在のインフラをそのまま使える。 ・白金触媒不要。 ・高温作動。ヒートサイクルの性能劣化。 ・部品材料がセラミックか材料が限られるため高価。デザインもある程度限られる。 ・起動時間が比較的長い。 同じSOFCの中でも、要求される性能は異なる。例えば工業用の大出力(数十~数百KW)のものは、基本的に運転しっぱなしであるため、高寿命、高効率さえ得られれば、起動時間が長くても、高温作動であっても問題にならない。自動車用APUについては、スイッチのON、OFFがあることから、ヒートサイクルの性能劣化が無いこと(低温化)、短い起動時間、軽量化などが要求される。 3.SOFCセルの構造 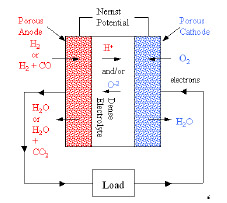 ・カソード(空気極)の反応:½O2 + 2e- → O2- ・アノード(燃料極)の反応:H2 + O2- →H2O + 2e- カソードで電子を受け取った酸素原子がO2-イオンとなり電解質に運ばれ、電解質材料と交換反応しながらアノードに到達し、ここで水素と結びつき電子を放出する。これが全体の電気の流れを作る。 ・カソード材料(空気極) 電解質まで酸素を通すためポーラスになっている。酸化による劣化が少ないことが条件。LSM/ La0.6Sr0.4MnO (lanthanum strontium manganite) 、LSC/La0.6Sr0.4CoO3 (Lanthanum Strontium Cobaltite)、SSC/Sm0.5Sr0.5CoO3(SSC)、LSCF /(La,Sr)(Co,Fe)O3などのMIEC(Mixed Ionic Electric Matrials = 電子性混合伝導体)が使われる。 ・電解質材料 酸素イオンの伝導性がいいことが条件(=酸化物)。ガスを通さないソリッド。YSZ/(Yttria stabilized zircornia)、ScSZ(Sc2O3-doped ZrO2 / スカンジア安定化ジルコニア)、ランタンガレート(LaGaO3)などのセラミック材料が使われる。 ・アノード材料(空気極) カソード同様、ガスを通すためポーラスになっている。NiO-YSZ、NiO-ScSZなどの、酸化ニッケルと(主に電解質材料と同様の)セラミックの複合材料が使われている。  上図(カソード、アノードの化学反応)の通り、アノード材料、カソード材料は電解質-ガス界面での電気触媒的な効果も要求され、また電解質との熱膨張係数の乖離があってはいけないことから、材料選定は限られてくる。 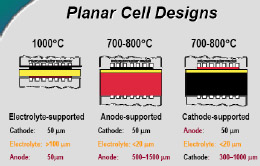 また、平型SOFCの場合には電解質を厚くした電解質支持セル(ESC=Electrolyte-Supported Cell)、アノードを厚くしたアノード支持セル(ASC=Anode-Supported Cell)、カソードを厚くしたカソード支持セル(CSC=Cathode-Supported Cell)がある。この他、アノードの下にポーラス金属の層を入れた、メタルサポートセル(MSC=Metal-Supported Cell)というものもある。また、アノードやカソードを2層にしたものもあり、それぞれポーラス率が違う(ガスの均一分散を図るため、通常は電解質に近い方がポーラス率が低い)。 セルを重ね合わせて高出力にしたものが「スタック」で、特に平型SOFCの場合にはセルとセルの間に、金属またはセラミックの「インターコネクタ(セパレータ)」が用いられる。円筒型SOFCの場合には、インターコネクタはセラミックの場合が多い。 さらに、スタックをまとめたものを「モジュール」と言い、例えば「1.5kwモジュール」など、ある電力を一単位としてモジュールを形成する。単数または複数のモジュールに燃料ガス改質装置、熱交換器、タービンなどをまとめたもの全体が、「SOFCシステム」になる。 4.SOFCシステムの構造 下図に一例を示す。セルの排熱でタービンを回すハイブリッド発電のもの。 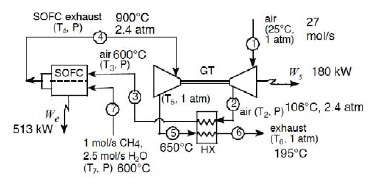 メタンと酸素と反応させる場合、理論的には800kj/molのエネルギーが発生するが、燃焼の場合には265kJ/molのロスが発生するのに対し、SOFCでは96kJ/molのロスしか発生しない。SOFCシステム内ではセルの温度が一番高く、その排熱を利用してメタン改質、タービン発電などを行う形が一番効率が良い(他の温度が高いということは、その部分を燃焼で温度を上げているか、外からエネルギーを持ち込んでいるということになり、システムの効率を低くしていることを意味する)。 その他セルから出た残留燃料ガスを触媒を用いて燃焼させたり、セルの排熱を改質機や温水生成に利用するなどの方法があるが、いずれにしてもセルの温度が一番高いということは変わらない。 SOFCの開発の上で長寿命、高効率が重要と言えるが、これには運転温度が深く関わってくる。SOFCの運転温度は500~1000℃の範囲で収まると考えられている。理由としては1000℃を超えるとセル材料の劣化が激しくなってしまい、加えて周辺部品の材料選定も限られて高価になってしまうこと、500℃を下回ると電解質のイオン交換反応が極端に落ちて、また低温であることから熱交換による改質(例:メタン→水素)がうまくいかなくなってしまことが挙げられる。運転温度については、下記の通りまとめられる。 ■ SOFC運転温度-高温時の長所、短所 ・電流密度が高い。(電気が良く流れる) ・改質に適している(メタン→水素の改質は吸熱反応のため高温の方が効率が良い)。 ・材料選定が限られる。高価になる。 ・材料劣化が比較的早い。 ・材料強度が落ちるなど、比較的扱いづらい。 ・電解質などの抵抗値が上がる。 ■ SOFC運転温度-低温時の長所、短所 ・いろいろな材料選定が可能で、安い材料を選択可能。 ・材料劣化が比較的遅い。 ・材料強度を保てるなど、扱いが比較的容易になる。 ・電解質などの抵抗値が下がる。 ・電流密度が低い。(電気が良く流れない) ・改質に適していない。 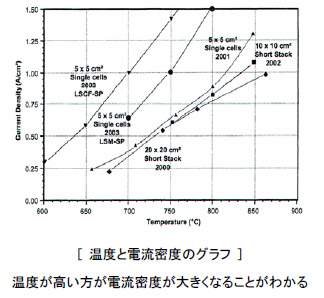 5.平型(Planar) SOFCと円筒型(Tubular) SOFCの構造と特徴 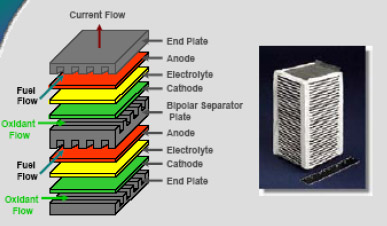 平型SOFCはアノード、電解質、カソードと重ね合わせてセルを構成し、インターコネクタを挟んで何層も積み重ねて高出力を得る構造。システム内のガスが漏れないように、ガラスシーリングで密封することが必要。 セルとインターコネクタとを別々に重ね合わせてガラスシーリングをする方式が一般的だが、数セル分まとめて焼結して、スタックを製造する方法もある。平型SOFCのインターコネクタ材料は金属が一般的(セラミックより抵抗値が低く、強度が高い)。ただ、セラミックのものも存在する。 なお、計算上1枚ものも200枚ものも、セルの総有効面積が同じで、ガスのフローや1枚あたりの電圧が同様であれば、理論上出力は同様である。 <計算ベース> 出力:10kW (10000W) セル電圧典型値:0.7V/cell 電流密度典型値:1A/cm2 <1枚ものの場合> I = W/V = 10000[W]/0.7[V] = 14300 [A] Area = I / Current Density = 14300 [A] / 1[A/cm2] = (120 cm)2 <200枚ものの場合> I = W/V = 10000[W]/(0.7[V] x 200 [cell])= 71[A] Area = I / Current Density = 71 [A] / 1[A/cm2] = (8.4cm)2 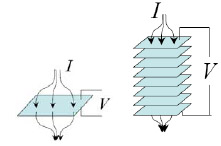 ※セルを重ねると、電流(I)は変わらないが、電圧(V)は増える。乾電池の直列をイメージすると分かり易い。 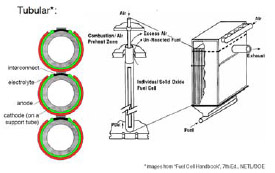 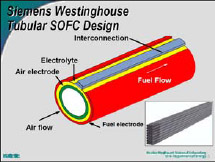 円筒型SOFCは筒の中に空気(カソード)、筒の外に燃料ガス(アノード)を触れさせる形になっている(筒の中に燃料ガス、筒の外に空気という逆の場合もある)。長さは75cm~1.6mのものまで、システムによって様々だがシームレスであることも円筒型SOFCの特徴である。また、円筒の先端が閉じている形状が一般的。 一般的な製法としては、最内層を「押し出し」した後、スラリーコーティングやAPS(プラズマ溶射法)で層を形成していく。材料はインターコネクタを含めて、全てセラミック材料の場合がほとんど。 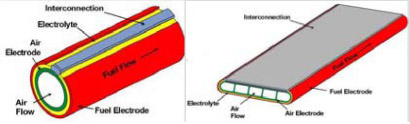 また、円筒を押しつぶしたような「フラットチューブラー」と呼ばれるタイプもある。これはガスに触れる面の割合やインターコネクタの面積を大きくして、効率を上げたもの。新しいものでは、チューブが3角形のものまである(Siemensの最新型)。基本的にフラットチューブラーは円筒型SOFCの改良型なので、製法や材料が円筒型と同様なものが多い。Siemensのフラットチューブラーはオールセラミックだが、今後の形状や製法の進化により、金属が使われる可能性もゼロではないだろう。 平型SOFC、円筒型SOFCの長所、短所を下記の通りまとめる。 ■ 平型SOFCの長所、短所 ・電力密度が高い。 ・円筒型に比べて製造コストが安い。 ・ガスに触れる面が大きく、大量の電流を流すことができる。 ・シーリングが必要。 ・高温強度に不安。 ■ 円筒型SOFCの長所、短所 ・ガスのフローが直線的で安定。 ・円筒という構造上、強度が高い(高温下でも)。 ・シーリングが不要(シームレス)。 ・平型に比べて製造コストが高い。 ・電力密度が低い。 ・インターコネクタやガスに触れる面の面積が小さく、平型に比べてロスが大きい。 6.SOFCの燃料 定置型(stationary)の場合には都市ガスが考えられている。日本の都市ガスは13Aという規格のものが一般的で、成分はメタン(CH4)70~80wt%、エタン(C2H6)10wt%未満、プロパン(C3H8)10~20wt%、ブタン(C4H10)10wt%未満を混合したものである。一例として、メタンの改質反応は以下の通り(改質には水分が必要)。 CH4+H2O → CO + 3H2 (SMR = Steam Methane Reforming) CO+H2O → CO2+H2 (WGR = Water-Gas Shift Reaction) この反応は高温の方が効率が良い。また、低温時にはカーボンの析出が問題になることもある。(下式参照) 2CO → CO2+C (Carbon Precipitation) また、都市ガスの上記主成分は無色、無臭であることから、ガス漏れの際に人の嗅覚でわかるよう、硫黄(S)原子の入った分子からなる匂いのある成分を入れている。そのため、アノード側のNiがSと反応して電圧を下げる、「硫黄被毒(Sulfur Poisoning)」と言われる現象が起きてしまう。これを軽減するため、運転温度を高温にしたり、電解質にスカンジア(Sc2O3)をドープしたジルコニアを使用する方法がある。また、脱硫装置を別途備え付ける場合もあるが、ここにエネルギーを使う分システムの効率が下がってしまう。 改質は改質装置で行う方法(SOFCの排熱を利用)、SOFCセル内で直接改質させる方法などがあるが、どちらにしても改質に関しては高温の方が都合がいいと言える。 都市ガス以外にも、石炭ガス、ガソリン(主にAPU向け)、軽油(APU、軍事向け)、ジェット燃料(飛行機向け)なども、SOFCの燃料として考えられている。いずれもSOFCならではの高温での改質のし易さがあるからこそ。 7.SOFC関連グラフ   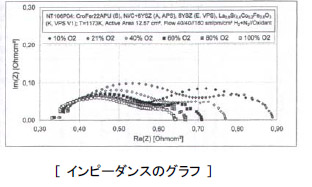 8.SOFCの課題点と解決方法 ・システムとして目標の4万時間(約4.5年)運転まで実現できていない。(Siemensの100kWのシステムが12000時間まで性能が落ちていない。あと3年で40000時間到達か?) ・カソード(空気極)のCr被毒による電圧の低下。(金属インターコネクタへのコーティングが有効。セラミックインターコネクタでは発生しない) ・アノード(燃料極)のS被毒による電圧の低下。(運転温度を上げる。脱硫装置を取り付けるなど) ・アノードでの直接メタン改質法が確立していない。(C-H結合を分解できるような触媒の開発が必要。Pd-Niバイメタルなどのアイデアがある) ・インターコネクタ材(Fe、Crなど)がアノードに入り込み、アノード材(Ni)がインターコネクタ材に入り込んでしまう。アノードの触媒作用がなくなり、化学反応が促進されなくなってしまう。(インターコネクタにNiOをコーティングするなどのアイデアがある)
・SOFC(固体酸化物形燃料電池)の基礎知識 ・SOFC(固体酸化物形燃料電池)の関連単語の日本語-英語対応表 ・燃料電池車(FCV)とSOFC(固体酸化物形燃料電池) ・ホームへ |
